moderator bandの項で紹介したように、心臓には単に収縮するだけではない、「調整する構造」が存在します。私は単離心筋細胞の収縮力を測定する研究に関わっていますが、そこで常に感じる疑問があります。
「心筋細胞は、本当にどこでも同じなのか?」
ここで興味深い論文をご紹介します。
Khokhlova A, Solovyova O, Kohl P, Peyronnet R.
Single cardiomyocytes from papillary muscles show lower preload-dependent activation of force compared to cardiomyocytes from the left ventricular free wall.
J Mol Cell Cardiol. 2022;166:127–136.
この研究では、ウサギの左室から以下の3つの部位、すなわち乳頭筋(papillary muscle)、心内膜側(endocardium)、心外膜側(epicardium)から心筋細胞を単離し、極細のカーボンファイバーを細胞の両端に接触させて収縮力を測定しています。
電気刺激により収縮した際のファイバーのたわみ量から力を算出し、さらにファイバー間距離を変化させることで前負荷を与え、収縮力の変化を評価しています。
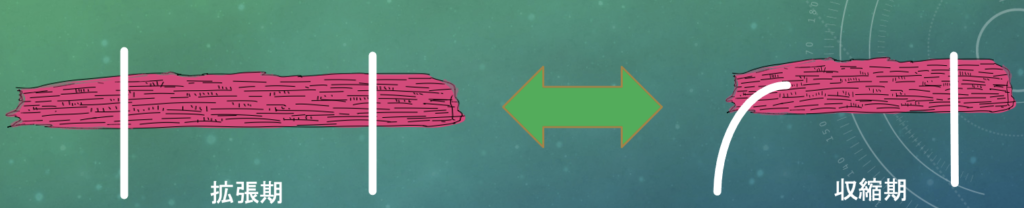
この方法により、以下の指標が測定されました。
- Caトランジェント:一過性の細胞内カルシウム濃度上昇。心筋細胞の収縮と弛緩のタイミングを決定する基本的なシグナルです。
- Frank-Starling Gain(FSG):細胞を伸展させた際にどれだけ収縮力が増加するかを示す指標です。収縮時の力の増加を拡張時の受動的な力で補正することで、純粋な長さ依存性収縮の強さを反映します。
その結果、乳頭筋由来の心筋細胞は、自由壁と比較してFrank-Starling応答が弱いことが示されました。
興味深いことに、この違いはカルシウム動態の差では説明できず、ミオシンフィラメントレベルでの力学的応答の違いによるものと考えられています。
この「機能に応じた力学特性の違い」という概念は、右室のmoderator bandにも共通する可能性があります。
moderator bandもまた強い収縮を担う構造ではなく、伝導と構造支持を通じて心室全体の機能を調整する役割を持っています。
すなわち、心臓におけるtrabeculated structureは、単なる筋肉ではなく、機能調整のために特化した構造であると考えられます。
単一の心筋細胞を調べることで、心機能そのものを直接評価することは難しいかもしれません。しかし、それぞれの細胞が持つ力学的特性は、心臓という臓器を構成する重要な要素であり、その組み合わせによって全体の機能が成り立っています。
むしろ重要なのは、「どの細胞がどのような特性を持っているのか」を理解することです。それが将来的には、新たな機能評価や治療戦略につながる可能性があります。
著者らは、これらの差は偶然ではなく、それぞれの構造が担う機能的役割に適応した結果であると考察しています。すなわち、血液を駆出する自由壁では高い、長さ依存性収縮が必要である一方、弁機能を支える乳頭筋では過度な収縮変動はむしろ不利であり、安定した動きが求められると考えられます。

コメント